
电话:029-87679000(总机)
地址:陕西省西安市西五路157号
邮编:710114
网址:www.2yuan.xjtu.edu.cn

电话:029-87679000(总机)
地址:陕西省西安市西五路157号
邮编:710114
网址:www.2yuan.xjtu.edu.cn

肺癌已成为严重威胁人类健康的重大公共卫生难题。非小细胞肺癌(NSCLC)作为其最主要类型,虽然受益于抗PD-1/PD-L1免疫疗法的应用,部分患者显示出卓越疗效,但肝转移的发生仍是导致免疫治疗效果严重减弱的关键挑战。肝转移微环境通常呈现出对免疫治疗不敏感的“冷”肿瘤特征,表现为CD8+ T细胞浸润缺乏和肿瘤细胞免疫原性低下,极大限制了治疗效果。尽管已有如IDO抑制剂等生化干预手段尝试改善此状况,但其临床成功率有限,暗示着存在其他更关键的调控机制亟待探索。
近年来,肿瘤物理微环境(TPME)在肿瘤起始、发展及治疗应答中的核心作用日益凸显,其对肿瘤免疫微环境(TIME)的调控也受到广泛关注。然而,在NSCLC肝转移的特定病理生理过程中,原发灶与转移灶之间由于器官特异性(如周期性拉伸的缺失和ECM硬度的显著增加)所带来的TPME差异,其如何协同调控TIME并最终影响免疫治疗的敏感性,目前仍不完全清楚。因此,迫切需要深入揭示这种器官特异性TPME在NSCLC肝转移免疫治疗低反应性中的调控机制,为开发新型有效的增敏策略提供理论基础和靶点。
西安交通大学第二附属医院肿瘤内科郭卉教授团队与西安交通大学生物医学工程与生物力学中心(BEBC)徐峰教授团队与等人揭示了一种创新的免疫治疗增敏策略,通过激活机械敏感离子通道Piezo1,可以有效克服非小细胞肺癌(NSCLC)肝转移的免疫治疗抵抗。研究发现,Piezo1的机械或生化激活能够诱导YAP核转位,通过FAK-YAP信号轴同时上调PD-L1表达和CXCL10分泌,将肝转移病灶从"冷"肿瘤转化为"热"肿瘤。更重要的是,研究揭示了循环拉伸可以改变ECM硬度对PD-L1/CXCL10的调控模式,从双峰分布转变为单峰分布,阐明了器官特异性物理微环境异质性影响免疫治疗响应的机制。相关工作以"Piezo1 Activation Improves NSCLC Liver Metastasis Immunotherapy by Overriding Matrix Stiffness-Mediated Bimodal PD-L1/CXCL10 Regulation"为题,发表在国际Top期刊Advanced Science上。

文章基于肺癌肝转移免疫治疗疗效差这一重大临床问题,肺癌原发灶与肝转移灶之间肿瘤物理微环境的显著差异是导致免疫治疗效果迥异的关键因素,并深入探讨了这些机械信号如何协同调控肿瘤免疫微环境(TIME)。研究结果具有一定临床转化价值,明确了机械敏感离子通道Piezo1作为非小细胞肺癌(NSCLC)肝转移免疫治疗的潜在新靶点。激活Piezo1有望成为一种新的治疗手段,以改善当前免疫治疗效果不佳的困境。
文章从多学科视角解决临床难题,是临床医学与生物力学、生物材料学等工程学科交叉合作的典范。工程技术的应用使得研究人员能够精确模拟和定量调控肿瘤细胞所处的物理微环境因素,如使用原子力显微镜(AFM)测量组织硬度,利用水凝胶技术构建具有特定刚度的细胞培养底物。这为深入探究TPME与肿瘤行为及免疫应答之间的构效关系奠定了基础。通过引入工程学的概念和技术手段(如构建体外周期性拉伸加载平台、运用数学模型等),为理解肿瘤免疫治疗抵抗这一复杂的临床问题提供了全新的研究视角和解决方案。该研究通过调控细胞的力学微环境或靶向力敏蛋白(Piezo1)来改善肿瘤免疫治疗效果,体现了“力医学 (Mechanomedicine)”这一新兴交叉领域的核心思想。这种医工交叉的合作模式不仅加深了对疾病发生发展机制的理解,也为开发基于物理生物学原理的新型诊断和治疗策略(如靶向TPME)开辟了道路。
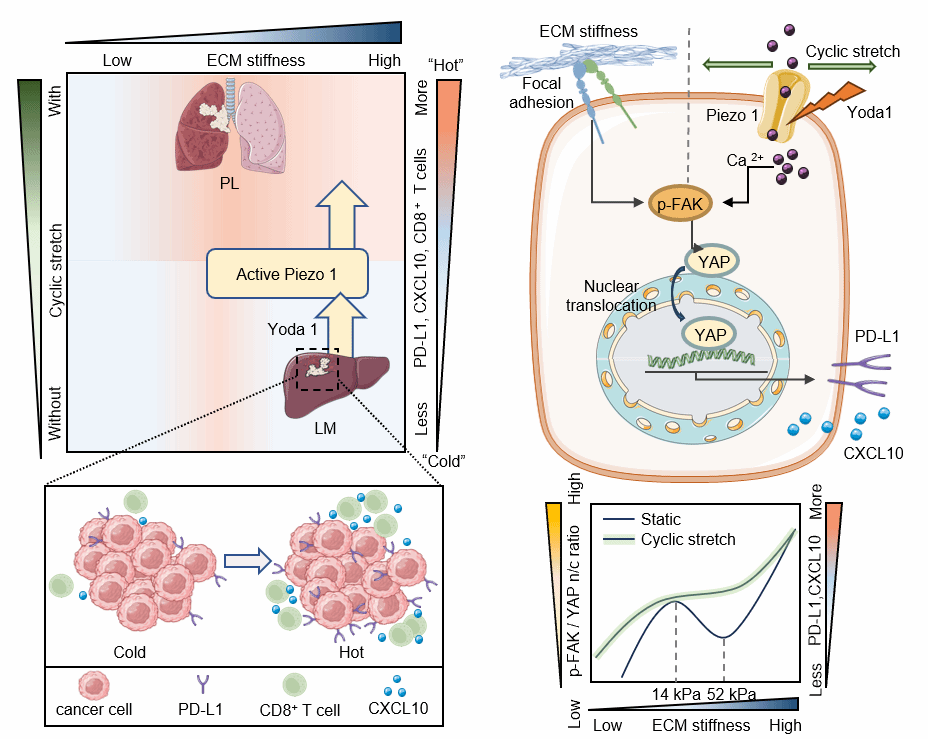
本文主要机制示意图